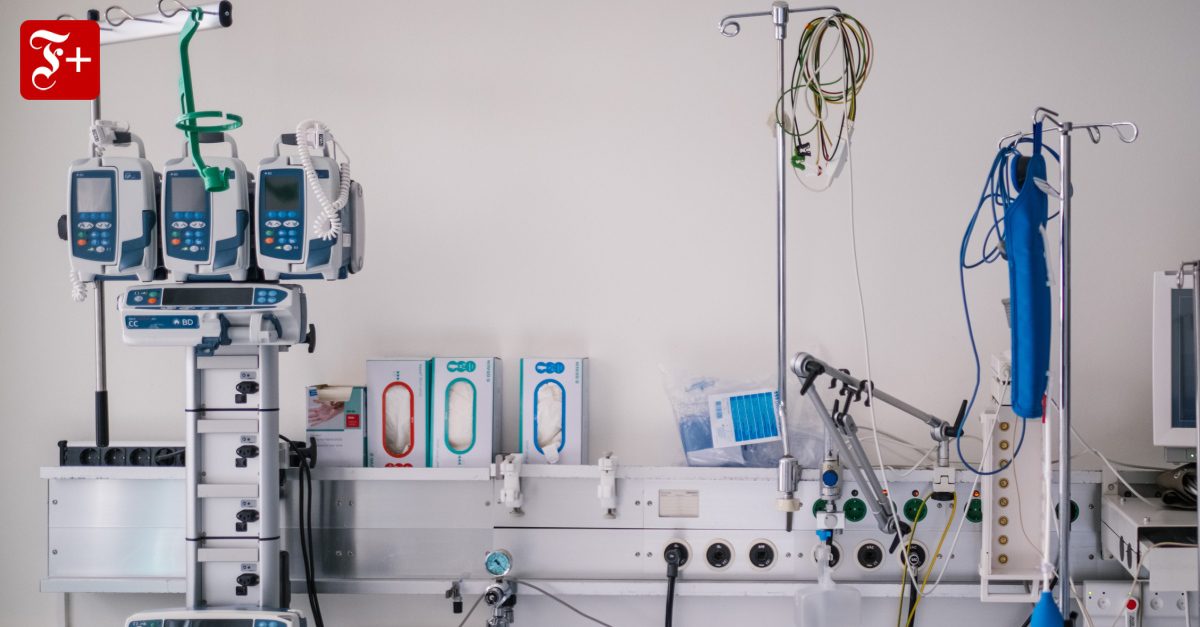
Tubos, bombas y cánulas: durante mucho tiempo, las reglas de prueba para dispositivos médicos han sido relativamente laxas.
Imagen: Picture Alliance
Después de numerosos escándalos de dispositivos médicos, la UE establece estándares más estrictos. Médicos y clínicas advierten. Ves la innovación y la oferta en peligro, el sentimiento de los demás.
S tMiden constantes vitales, permiten operaciones difíciles, aseguran una vida diaria tolerable o supervivencia: productos médicos como ventiladores, stents, instrumentos quirúrgicos o camillas y yesos. Dispositivos indispensables, entonces, y sin embargo siempre hubo escándalos: roturas de cables y descargas eléctricas en desfibriladores implantados, daño tisular por abrasión metálica de prótesis o stents, tras cuyo uso se producían múltiples descargas. El fabricante francés PIP incluso ha utilizado criminalmente silicona de calidad industrial inferior en decenas de miles de implantes mamarios, posiblemente con consecuencias fatales para algunas mujeres.
Las normas anteriores de la UE eran bastante laxas. Los marcados CE necesarios no los emiten las autoridades, sino los organismos notificados: empresas que están acreditadas para ello. Pero a veces trabajaron descuidadamente, los periodistas del British Medical Journal recibieron comentarios positivos sobre documentos problemáticos para productos inventados. Una razón: los centros de pruebas no tenían que contratar expertos médicos y están interesados en los pedidos. Tampoco tenían que inspeccionar la producción sin previo aviso.